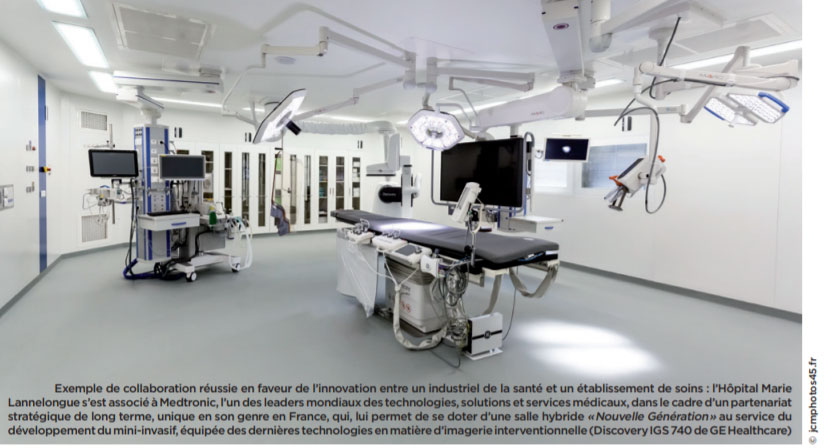
Avec notamment la moitié de la recherche académique nationale, la majeure partie des centres r&d concentrés sur son territoire, le plus grand réseau hospitalier et un riche tissu de PME tant dans le secteur des dispositifs médicaux que des biotechnologies, la filière francilienne de la santé et des sciences du vivant, est aujourd’hui la première en Europe.
Le palmarès est impressionnant. La région compte plus de 1 000 établissements pharmaceutiques, dont l’ensemble des grands laboratoires français (Sanofi, Pierre Fabre, Servier, Ipsen, Guerbet…) qui côtoient les grands laboratoires internationaux : Pfizer, GSK, Novartis, Johnson&Johnson, Astra Zeneca ou Roche.
Elle est une terre d’accueil pour les entreprises les plus innovantes en matière de biotechnologie avec plus de 200 sociétés implantées, des incubateurs et bioparks comme le Génopole, Paris Biotech ou Agoranov et a vu s’y développer les centres de recherche les plus avancés dans le domaine des technologies médicales : GE Healthcare, Siemens, Philips, B Braun Médical ou Sorin Medical, attirés par le plus grand réseau hospitalier d’Europe composé de 37 hôpitaux, accueillant 71 800 professionnels pour une capacité de 22 500 lits.
Une recherche de pointe
L’Ile-de-France concentre 300 laboratoires de recherche publics et privés, 11 800 chercheurs dont 4 400 dans l’industrie, et des organismes prestigieux de renommée internationale comme l’Institut Pasteur, l’Institut Curie, l’Institut Gustave Roussy, le CNRS, l’INSERM, le CEA, l’INRIA, l’INRA, … dans la filière des sciences du vivant.
Des formations d’élite (9 universités et 20 grandes écoles) lui assurent un très haut niveau de qualification. La région est également le leader européen des essais cliniques, 850 essais cliniques sont réalisés chaque année sur 20 000 patients et 2 800 projets de recherche sont en cours. Le pôle de compétitivité MEDICEN, animateur régional de la filière santé, est le lieu unique où travaillent ensemble PME et startups, grands acteurs industriels, recherche académique et professionnels de santé pour créer de la valeur économique et mettre sur le marché des solutions innovantes au service de la santé des citoyens et des patients.
Fin 2017, ce pôle qui compte 345 membres dont 290 PME, avait ainsi initié 302 projets labellisés représentant un investissement de 1,32 Mds € qui ont permis l’émergence de 137 solutions dont 68 produits déjà sur le marché. Une innovation territoriale dans une approche internationale au sein d’un réseau national de 7 pôles de compétitivité qui travaillent ensemble sur la santé pour faire reconnaître les spécificités et la richesse de cette filière en France, ainsi que son positionnement stratégique.
MEDICEN accompagne ainsi ses adhérents dans leur développement à l’international.
Des innovations au cœur des attentes des patients
En 2017, 15 nouveaux projets ont été labellisés, pour plus de 100 millions € d’investissements. Parmi les plus remarquables, le projet MyProbe vise à développer des outils efficaces pour identifier les risques élevés de rechute du cancer du sein et ainsi réduire l’utilisation de traitements supplémentaires lourds et coûteux pour les patientes.
KDT-Innov a pour but de prévenir la perte des greffons rénaux en améliorant le diagnostic du rejet, en prédisant le risque de perte du greffon à long terme et de réponse au traitement anti-rejet.
Smart Angel, porté par EVOLUCARE, a pour objectif de développer un écosystème numérique performant dédié à la surveillance et l’accompagnement des patients tout au long de leur parcours de soins mais aussi lors de leur retour à domicile.
NOVAPULSE quant à lui, vise à développer un nouveau type de pompe d’assistance cardiaque mini-invasive, permettant de prendre en charge les seniors touchés par l’insuffisance cardiaque chronique et non éligibles à l’implantation d’une assistance totale.
Des mesures pour renforcer l´attractivité de la France
En juillet dernier, le Premier ministre Édouard Philippe a pris la parole devant le conseil stratégique des industries de santé (CSIS), pour présenter des mesures favorables aux industries du médicament et du dispositif médical. Ces dernières années, le tissu industriel français a eu tendance à se contracter autour des médicaments de synthèse arrivés à maturité, alors que nos voisins européens attiraient les produits les plus innovants, les médicaments biologiques et les thérapies géniques.
Partant de ce constat, l’exécutif veut donner un signal positif en rendant le cadre plus attractif pour les essais cliniques, la production et la commercialisation des nouveaux médicaments, notamment les traitements innovants comme les nouvelles thérapies individualisées du cancer (CART). Le gouvernement promet notamment une accélération des procédures administratives.
Les délais médians pour démarrer un essai clinique devront être abaissés à moins de 45 jours par l’Agence nationale de sécurité du médicament et des produits de santé (ANSM), contre 51 aujourd’hui, et moins de 60 jours devant les Comités de protection des personnes (CPP), contre 85 aujourd’hui, sauf pour les thérapies innovantes.
Quant à l’accès au marché, qui passe par une évaluation par la Haute autorité de santé et la négociation du prix avec le Comité économique des produits de santé, il devra revenir aux 180 jours préconisés par l’Union européenne au lieu des 275 jours actuels pour un médicament non générique et plus de 500 jours pour un dispositif médical.
Par ailleurs, un soin particulier sera apporté aux thérapies cellulaires, des produits de pointe rares et onéreux dont les demandes d’autorisation d’essais cliniques seront traitées prioritairement (30 à 45 jours).
Une annonce bienvenue alors que plusieurs entreprises étrangères veulent pouvoir tester, produire et commercialiser leurs produits dans l’Hexagone.
Pour marquer leur approbation de ce nouveau climat, les grands noms du secteur ont déjà annoncé de nouveaux investissements dans notre pays. Sanofi va doubler sa participation dans deux fonds destinés à l’innovation, Merck MSD investira 80 millions d’euros d’ici à la fin de l’année notamment dans une soixantaine d’essais cliniques et dans les données de santé (10 millions d’euros).
De son côté Novartis a annoncé qu’il avait signé avec Cell4Cure, filiale du LFB pour produire dans l’Essonne pour l’Europe, ses traitements personnalisés du cancer comme Kymriah. Et Celgene qui va débuter un essai clinique avec un même type de produit, entend multiplier par deux son investissement en recherche clinique au cours des trois prochaines années.